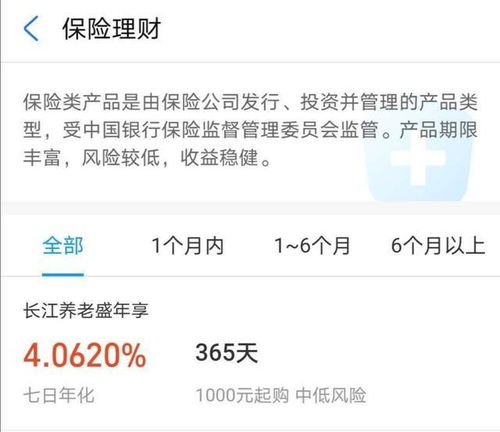
显著延缓高风险SMM进展亚虹医药获2家机构调研:PL-1706的上市申请已于2023年11月获国家药品监督管理局受理,公司正在积极推进其上市审评审批工作,并期望于2025年上半年获得上市批准(附调研问答)
1|0条评论

股市动态
MORE>-
12-12美国务院发言人拒绝评论美以通话只是“嘴上说说”?外媒:这是在发出继续战斗的邀请
-
12-12临床外显子组和基因组测序的次要发现ACMG SFv3.1列表
-
12-12我心目中的好老师作文
-
12-12答球迷:当年UFC和张伟丽比赛后,乔安娜的脸为何变形那么厉害?
-
12-12奥运会中国获得金牌一览表,奥运会中国获得金牌情况2021
-
12-12转发:安徽财经大学2022年硕士研究生招生考试复试录取办法
-
12-12李云泽锂电材料产业或迎来困境反转
-
12-12营收出现下滑财报速递:遥望科技2024年前三季度净亏损4.08亿元
-
12-12积分相同的球队如何决定排名?世界杯小组赛积分有多少种可能?
- 搜索
- 最近发表
-
- 美国务院发言人拒绝评论美以通话只是“嘴上说说”?外媒:这是在发出继续战斗的邀请
- 深度解析002302股票,理性投资的艺术与策略
- 让投资更有趣从拼技术到迈向商业化,中国AI大模型开启“竞速跑”
- 原创阿森纳3-0击败布莱顿,英超榜首表现惊人
- 看这5位军队女代表委员的履职风采
- 临床外显子组和基因组测序的次要发现ACMG SFv3.1列表
- 美国务院最新回应韩媒:美政府已“不信任尹锡悦”
- 运动幼儿园简笔画
- 我心目中的好老师作文
- 探索白银上市公司,走进这个闪闪发光的金融世界
- 绿茵2串1:葡萄牙克敌制胜 西班牙大胜可期
- 荣威RX5 MAX智驾健康舱守护出行
- 答球迷:当年UFC和张伟丽比赛后,乔安娜的脸为何变形那么厉害?
- 假期优化落地有望提振出行链假日经济“热”潮涌动 激发消费市场新动能
- 美元指数拉升非农数大超预期,美债收益率飙升、美元指数上扬
- 足坛超级大雷,陈戌源信仰崩塌拉儿子下水,爷俩在里面唱铁窗泪!
- 涿州市梅花鹿养殖国家政策拓展乡村生态产业 推动农业绿色发展
- 深度解析——股票002666,投资理财中的隐形冠军
- 莱克电气江苏苏州:绿色数智 打造轻工业发展新优势
- 奥运会中国获得金牌一览表,奥运会中国获得金牌情况2021
- 好理财,有配置——应对与机遇 | 理财嘉友记青岛站
- 转发:安徽财经大学2022年硕士研究生招生考试复试录取办法
- 董氏针灸调理【心脏】处方
- 都乐超甜蕉,果燃超带劲,都乐助力锡马十年燃情开跑
- 深度解析,600582天地科技,科技巨头背后的产业转型与机遇
- 纪实职业试药员:包吃包住7天赚10万!用命换钱真的值得么?
- 万秀区科技文化体育和旅游局 贫困村产业发展科技服务队工作情况汇报
- 火箭湖人交易得费舍尔 休城3人大交易得坎比 汇总
- 紧张和愤怒这两种情绪会影响人的健康吗
- 李云泽锂电材料产业或迎来困境反转
- 朱芳雨晒出全家福, 三个儿子重聚, 怀抱小儿子, 前妻胡美未现身
- 营收出现下滑财报速递:遥望科技2024年前三季度净亏损4.08亿元
- 深度解析,信立泰——医药界的创新引领者,潜力与挑战
- 理论上不兼容齐祖,现实中瞧不起德尚,曼联大佬在法国队自毁前程
- 顺义:“体育+经济”,后沙峪镇成为运动小镇
- 积分相同的球队如何决定排名?世界杯小组赛积分有多少种可能?